Géneké és elektromos kütyüké a jövő az orvoslásban
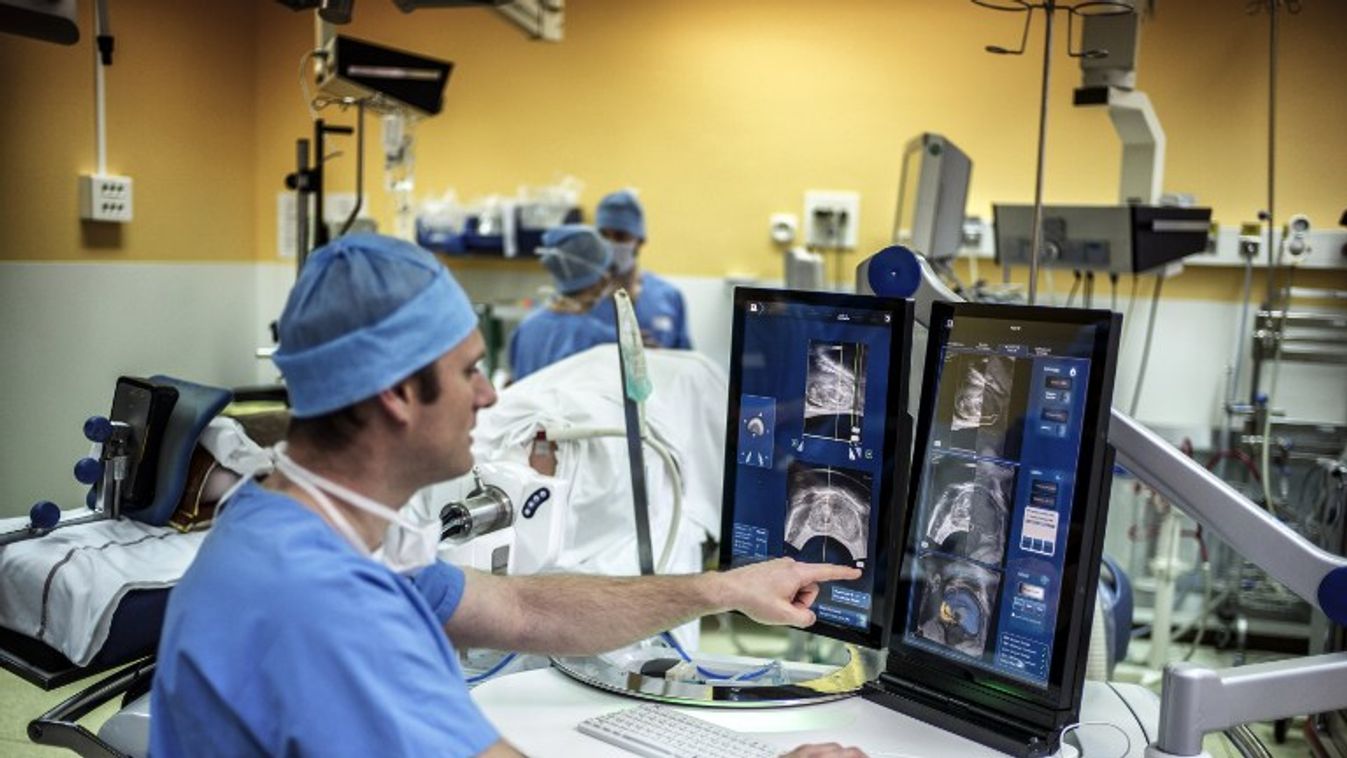

A modern biológia fejlődése mára elképesztő sebességre kapcsolt.
Szinte hetente bukkannak elő alapvetően új ismeretek és technológiák a tudományos műhelyek bugyraiból.
A kutatást nem csupán az öncélú megismerés motiválja, hanem a tudásunk gyakorlati alkalmazása is, melynek ma messze legfontosabb területe a gyógyítás.
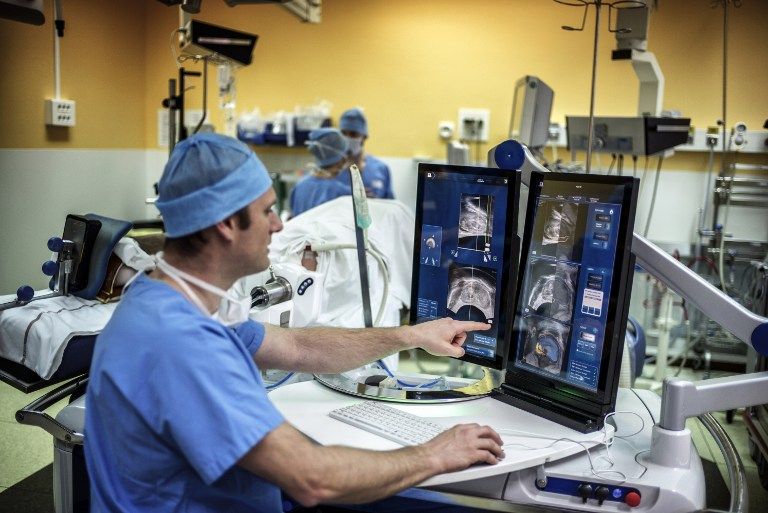
A tudományos fejlődés következtében a gyógyászat jelenleg többszörös paradigmaváltás előtt áll. Ma akkor megyünk orvoshoz, ha már megvan a baj.
A jövőben azonban megtudhatjuk előre, milyen kórokra számíthatunk, és így tehetünk is kialakulásuk ellen.
Nemsokára aktív módon közreműködhetünk a betegségeink felismerésében és a szükséges terápia kidolgozásában. Nem kell majd sorban állnunk sem a várólistákon, sem az orvosi rendelők előtt, e-páciensként intéződnek majd ügyeink, valós időben.

Nem lesz szükséges tájékozódnunk, hogy melyik dokihoz érdemes menni, mert az orvosi intuíció helyett számítógépek fognak diagnosztizálni,
és a terápiát illető döntéseket hozni azon paraméterek alapján, amelyeket a testünkön és a lakásunkban lévő elektromos kütyük produkálnak. Az egészségügy ma még a tömeg részeként kezel bennünket, nemsokára viszont eljön a személyre szabott gyógyászat kora.

Hatékony technológiákkal fogjuk leküzdeni a betegségeinket, ha a megelőzés és a folytonos kontroll ellenére mégis hatalmába kerítene bennünket valamilyen kór. Egy rendkívül érdekes világ közeledik, amelybe úgy folyunk majd bele észrevétlenül, mint ahogy az információs technológia szőtte át lopva a földgolyót.
A világ pusztán gondolati úton nem ismerhető meg, kísérletek és megfigyelések is szükségesek ehhez. A tudomány éppen így működik, ezért vált a tudás megszerzésének egyetlen hiteles módszerévé.

Az evidenciaalapú gyógyítás lényege, hogy csak az a terápia válik az orvosi praxis részévé, ami kiállta a szakszerűen elvégzett tesztek próbáját.
A tudományos alapokon nyugvó orvoslás azonban ennél lényegesen több: koherens keretbe helyezi az ismereteket, és magyarázatot is ad az egészséget érintő biológiai jelenségek hátterét illetően.
A modern gyógyítás óriási változások előtt áll, amelynek a molekuláris biológia a fő motorja. E tény hitelét még az a nyilvánosan soha be nem ismert skandalum sem veheti el, hogy
a Humán Genom* Projekt (HGP) indulásakor (1990) a kutatók alaposan átverték a közvéleményt.
A vezető tudósok ugyanis azt állították, ha megfejtjük az emberi DNS bázissorrendjét*, azzal egyben megismerjük a betegségek genetikai hátterét, sőt, gyógyítani is tudjuk majd azokat.

Ezzel a lódítással nyilvánvalóan az anyagi támogatás megszerzése volt a cél.
A HGP 14 év alatt három milliárd dolláros költséggel szekvenált* meg egyetlen emberi DNS-t. Ma ugyanez néhány órába és ezer dollárba kerül. Az utóbbi években nagy költségvetésű, államilag finanszírozott genomprogramok indultak be szerte a világon: Nagy Britannia százezer, az USA és Kína egy-egy millió emberi genom meghatározását tűzte ki célul. Az indíttatás minden esetben deklaráltan orvosi: a főbb betegségek genetikai hátterének feltárása.

Míg az egygénes betegségek* megállapítása viszonylag egyszerű (megvizsgáljuk, mutáns-e az adott gén), addig a kórjaink 98%-át kitevő úgynevezett komplex betegségek* genetikája ma még egy rendkívül nehéz feladat, mivel az ezek kialakulásához hozzájáruló génvariánsok nem oksági, hanem csupán hajlamosító tényezők.
A nyomorúságaink genetikai nyomainak felderítéséhez ezért rengeteg beteg és egészséges ember DNS-ét kell meghatározni,
és azokat összehasonlítva kiszűrni a releváns tényezőket. Ráadásul a feladatot tovább komplikálja az a tény, hogy a betegségek kialakulásához számos kedvezőtlen allél együttes előfordulása mellett megfelelő környezeti és életmódbeli hatások is szükségesek.
Ádáz vita uralja ma a genommedicinát, amelynek tárgya az, vajon az egyes betegségeket viszonylag kevés genetikai változat okozza-e (Gyakori Variáns Hipotézis; GYVH), vagy ezek hátterében több száz vagy ezer allélvariáns áll, ráadásul minden családi vonalnál egyedi genetikai háttérrel (Ritka Variáns Hipotézis; RVH). A GYVH jegyében folytatott kutatásokra költött jókora összegek eddig feltűnően szerény eredményeket szültek.

A hipotézis hívei szerint a sikertelenség oka, hogy a jelenleg rendelkezésre álló adatmennyiség még nem elegendő megbízható következtetések levonására.
A GYVH-en alapuló kutatási módszer lényege az, hogy a DNS-ünkben elégséges néhány genetikai markert (tipikusan egy-egy bázisban való különbségeket) találnunk, amelyek alapján meg tudjuk jósolni a főbb betegségeket. E genetikai markerek rendszerint nem is oki tényezők (nem az adott bázisvariánsok okozzák a betegséget), csupán jelzik, hogy a közelben egy hibás gén található.
Orvosbiológiai kislexikon
Bázissorrend: a DNS-t alkotó négy bázis (ATGC) sorrendje hordozza a genetikai információt.
A GYVH teoretikusai szerint azért lehetséges, hogy egy adott betegségre utaló markerek a DNS ugyanazon pontjain helyezkednek el, mert az emberi populáció létszáma néhány tízezer év alatt óriási méretűre duzzadt, és a szóban forgó genetikai mintázat szülőkről utódokra öröklődött.
A nagy darwini seprű pedig azért nem takarította ki a selejtes génvariánsokat, mert a komplex betegségek rendszerint csak nagyszülői korban jelentkeznek,
és ilyenkor már letudtuk evolúciós kötelezettségeinket a gyermeknemzést illetően.

A rivális RVH szerint azonban az új mutációk és az ivarsejtek képzésekor lejátszódó genetikai rekombináció családonként más-más genetikai háttérrel produkálják ugyanazokat a betegségeket, ezért a markereken alapuló módszer hasznavehetetlen.
Egy adott betegség genetikai tényezőit tehát csak igen nagyszámú DNS-szekvencia tanulmányozásával lehet megismerni,
és minden egyéni kórkép felállításához teljes genomszekvenálást és komoly bioinformatikát kell majd alkalmaznunk.
A DNS egy komplex hierarchián keresztül irányítja a testünk és az elménk működését, több-kevesebb szabadságot hagyva az egyes szinteken, mint amilyenek az RNS-ek, a fehérjék, a jelutak, a sejtek, a szövetek, a szervek, a szervrendszerek és maga a szervezet. A környezet hatásai általában nem közvetlenül a DNS-t, hanem a testet érik, de ún. epigenetikai* módosulások révén a gének kifejeződése is megváltozhat.

A betegségek predikciójához ezért nem elegendő a genetikai profil megállapítása, egy integrált profilt (IPOP*) kell alkotni, amely magában foglalja a DNS és az epigenetikai mintázatok mellett az RNS- és fehérjemolekulákat, az anyagcseretermékeket, a különféle biokémiai és élettani paramétereket, valamint a szervezetünkben élő baktériumokat (mikrobiom) és más hasonló tényezőket.
A probléma az, hogy - míg a DNS minden sejtben ugyanaz - a többi molekula szövettípusonként változik,
ezért elvileg mintát kell vennünk a vizsgálandó szervekből, ami gyakran nem egyszerű feladat.

Van azonban egy megoldás: a könnyen hozzáférhető szöveteink – elsősorban a vér – igen sok információt tartalmaznak a test egészségi állapotáról, ezért elegendő lehet, ha csak ezekből veszünk mintát.
Ma a vérből még csak tíz egynéhány paramétert vizsgálunk, a jövőben viszont e biomarkerek* száma milliós nagyságrendűvé válik.
A genombiológia mellett manapság nagy állami pénzeket lehet nyerni agykutatásra is.
A projektek ideológiájukban szintén a betegségek kutatását tűzik ki célul,
de néhány kivételével (Parkinson-kór, poszttraumás stressz stb.) nem közvetlenül ezeket vizsgálják, hanem az idegsejtek rendszerszintű kommunikációját, valamint azt, hogyan gondolkodunk, tanulunk és emlékezünk.

Az agy és elme betegségei érintik legfőképp emberi mivoltunkat, és ráadásul ezek terhelik leginkább az egészségügyi kasszát is, ezért mindenképpen indokolt a megkülönböztetett figyelem.
A génterápia több mint két évtizedig tetszhalott állapotban volt néhány balul kiütött klinikai kísérlet miatt, de a közelmúltban újraéledt, és máris sikereket ért el elsősorban az immunrendszer betegségei és Parkinson-kór elleni harcban. E technológia máig tabu területe az úgynevezett csíravonal-génterápia, amely során nem pusztán az érintett szövetekben, hanem a test összes sejtjében megváltoztatjuk az örökítőanyagot.
A tiltakozások általában misztikus attitűdök által motiváltak, például: ne avatkozz be a természet rendjébe vagy a Teremtő alkotásába. Hasonló az ellenérzések alapja az őssejtterápiával kapcsolatban is: mivel az eredeti technikához petesejt vagy mesterséges megtermékenyítéssel létrehozott embrió szükségeltetik, sokan gyilkosságnak tekintik a protokollt.
Az ún. indukált pluripotens őssejtekre* alapozott terápia képes kivédeni az etikai aggályokat, mivel itt differenciált sejteket alakítanak vissza őssejtekké az epigenetikai memória törlésével.
Senki nem állíthatja, hogy egy kötőszöveti sejt felhasználásával potenciális emberi életeket ontunk ki.
Ráadásul, e technikával saját sejtjeinket is használhatjuk a gyógyításhoz, elkerülvén így az immunológiai összeférhetetlenséget. Az őssejtek 3D-s nyomtatása lehetővé teszi, hogy akár a testünkbe ültethető szerveket is előállíthassunk.
Az apró kütyük a gyógyászat fontos segédeszközei lesznek. Nanomembránokat alkalmazhatunk például idegen eredetű inzulint termelő sejtek védelmére az immunrendszerünkkel szemben. A nanokagylók toxikus hatású anyagokat szállíthatnak a rákos sejtekhez.
Nagy oxigénkötő kapacitással rendelkező respirociták állíthatók elő a vörösvértestek helyettesítésére baleset vagy vérszegénység esetében. Mesterséges fehérvérsejtek intézhetik el a kórokozókat.
Később a vérünkben keringő nanoszenzorok tudósítják majd számítógépeinket az egészségi állapotunkat illetően.
Az új tudományos és technikai vívmányok alapvetően át fogják alakítani a közeljövő orvoslását. Nézzük meg, miként.
A jelen gyógyászata reaktív, ami annyit jelent, hogy csak a betegség megjelenését követően foglalkozik a beteggel. A proaktív (megelőző) gyógyítás a páciensek folyamatos vizsgálatán alapul.
A genetikai és egyéb profilok alapján jóslatokat lehet tenni a különféle betegségek kockázatát illetően,
ami alapján - szükség szerint - megelőző beavatkozások vagy rendszeres időközi vizsgálatok végezhetőek, valamint életmódbeli tanácsokkal lehet ellátni a pácienseket.
A jelen tömegszemléletű gyógyászata gyakorlatilag nem tesz különbséget a betegek között, mindenki egyforma terápiát kap egy adott bajra.
Ezzel az a probléma, hogy egy kezelés bizonyos páciensekre nem hat, másoknál viszont súlyos mellékhatásokat okoz.
Évente világszerte 850 milliárd dollárt költünk gyógyszerekre, ebből 370 milliárdot hatástalanokra.

A forgalomban lévő szerek 70-80%-a ugyanis csak a betegek 40-50%-ára hat. Ma Európában és az Egyesült Államokban a gyógyszerek mellékhatása által okozott halál az 5-6. helyen áll, ami megdöbbentő szám. Ezen a helyzeten fog változtatni a személyre szabott gyógyászat.

A különböző profilok alapján képesek leszünk megállapítani, hogy mely kezelések lehetnek számunkra hatásosak, egyben mellékhatásmentesek.
Az ún. szekvenciaspecifikus gyógyszerek (DNS, RNS, fehérje, antitestek) és az őssejtek alkalmazása lesz a személyre szabott gyógyítás legfőbb eszköztára.
Jelenleg a páciensek passzív résztvevői a gyógyításnak, a jövőben az informált részvétel fog dominálni. Az információkat megbízható internetes oldalak látogatásával fogják megszerezni a páciensek, akik segítenek a diagnózisuk megállapításában és a terápia kidolgozásában is.

Ma az internetes tájékozódás nem ajánlott, mivel a laikusok gyakran alapvető ismeretekkel sem rendelkeznek az egészség biológiai alapjait illetően,
valamint a szabadon garázdálkodó átverés téves információkkal árasztja el a hálót, az ezek alapján való döntés tragikus kimenetelű is lehet.
A betegvárók zsúfoltságát megszüntetik majd az e-páciensek, akik az interneten kommunikálnak orvosukkal. A testükön és a lakásukban lévő különféle eszközök fogják az orvos számítógépe felé közvetíteni az egészségi állapotuk paraméterei.

Szemben a jelenlegi intuitív orvosi döntésekkel, a jövőben a különféle biomarkerek és profilok alapján egy számítógépes szoftver állítja majd fel a diagnózist,
és javasol döntést. Érdekessé válik az orvos szerepe a digitális medicina korában.
A hagyományos gyógyászat jelenleg számos nehézséggel szembesül. Az egyik, hogy jelen tudásunk korlátozott volta miatt nem ismerjük fel időben, és nem is tudjuk hatékonyan gyógyítani betegségeink jelentős hányadát. A másik probléma, hogy szereink egészségkárosító mellékhatása ma még túlságosan nagy.
Egy további gondot az egy páciensre jutó korlátozott idő jelenti.
Végül, de nem utolsósorban, két ellentétes tendencia fut ma egymással versenyt: az adott technológiaszint egyre olcsóbb reprodukálása és az új technológiák folyamatos megjelenése. Mivel az utóbbi gyorsabb ütemű, különbségük az egészségügy nettó drágulását okozza. A közeljövő e problémákat orvosolni fogja.

Az új típusú gyógyszerek engedélyeztetési gyakorlatának meg kell azonban változnia, hiszen személyre szabott terápiák kifejlesztésére egyetlen gyógyszergyár sem fog több százmillió dollárt és tíz évet befektetni.
Az új világ új embertípust is kíván: nem elegendő, ha a tudás privilégiumával csupán egy szellemi elit rendelkezik,
mindannyiunknak el kell sajátítania a természettudományok és a racionális gondolkodás alapjait.

Ebben a korban az alternatív orvoslásként ismert átverés magától megszűnik majd, mivel a tudás felszántja a hiszékenység táptalaját. A fenti forgatókönyv megvalósulásának van azonban egy feltétele:
a mát domináló irracionalizmus nem győzheti le az értelmet az új korszak beköszöntése előtt.
A tudatlanság ugyanis képes visszataszítani civilizációnkat a történelmi sötétség ölelő karjai közé.











