Döntött az EU: forgalmazható a Johnson & Johnson vakcinája

Ez a negyedik vakcina, amely az Európai Unió gyógyszerfelügyeleti hatóságának szerepét betöltő ügynökség ajánlása szerint hatékony a SARS-CoV-2 koronavírus ellen, de az első, amely egydózisú.
Az uniós ügynökség közleményében az áll: az EMA Humángyógyszer Bizottsága (CHMP) gyorsított eljárás keretében végezte a Johnson & Johnson COVID-19 Vaccine Janssen nevű oltóanyag vizsgálatát, amelynek során értékelte a vakcina hatékonyságára és biztonságosságára, valamint minőségére vonatkozó, már rendelkezésre álló adatokat. Alapos értékelés során az EMA illetékes bizottsága arra a következtetésre jutott, hogy
a vakcinára vonatkozó adatok megbízhatóak és megfelelnek a kritériumoknak, az oltóanyag azonnali rendelkezésre állásából származó előny egyértelműen meghaladja a gyógyszerrel összefüggő kockázatokat.
A rövidített értékelési folyamat azért volt lehetséges, mert az EMA korábban már megkezdte az oltóanyag folyamatos felülvizsgálatát.
Az amszterdami székhelyű EMA ez idáig a Pfizer amerikai gyógyszergyártó és partnere, a BioNTech német biotechnológiai cég által kifejlesztett vakcinát, a Moderna amerikai biotechnológiai vállalat oltóanyagát, valamint az AstraZeneca gyógyszeripari vállalat és az Oxfordi Egyetem által közösen kifejlesztett oltóanyagot ajánlotta forgalmazásra.
Az EU-s ügynökség mind a négy esetben gyorsított eljárás keretében hozta meg döntését, amely
az oltóanyag egyéves feltételes alkalmazásához adja meg a zöld jelzést.
Azt is közölték, hogy a feltételes forgalombahozatali engedély megadását célzó eljárás során a gyógyszerre vonatkozó vizsgálat a szokásoshoz képest kevésbé átfogó adatok alapján történik. Az engedély megadását követően a vállalatoknak bizonyos határidőn belül további, többek között a folyamatban lévő vagy új vizsgálatokból származó adatokat kell szolgáltatniuk annak megerősítésére, hogy az előnyök továbbra is meghaladják a kockázatokat.
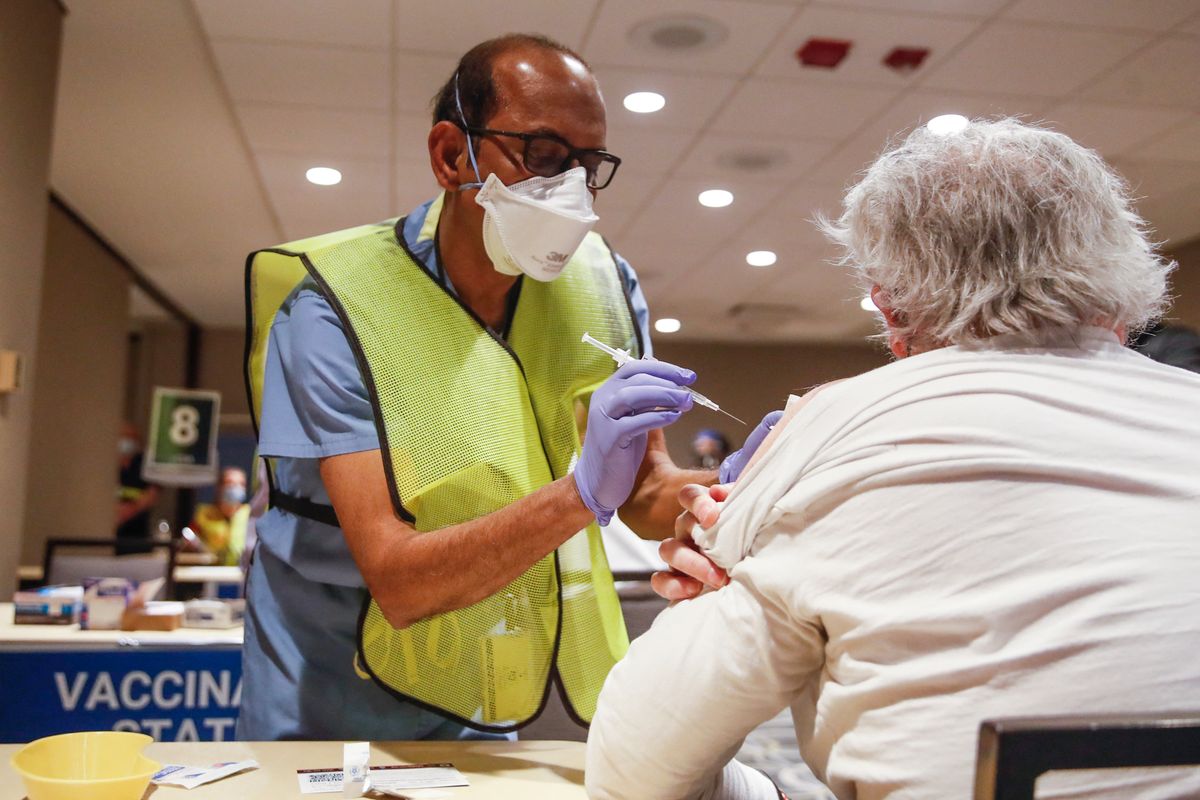
A Johnson & Johnson oltóanyagában ártalmatlanított adenovírussal juttatják be a koronavírusra jellemző tüskefehérjét a szervezetbe.
Az immunrendszer ezt követően idegen anyagként kezeli ezt a fehérjét, és természetes védekezésként antitesteket és a fehérvérsejtek csoportjához T-sejteket termel ellene.
Közölték, hogy
a vakcinában található adenovírus nem képes szaporodni, és nem okoz betegséget.
A már felhasználásra ajánlott oltóanyagokat gyártó vállalatok mellett ez idáig az orosz Szputnyik V fejlesztői kértek hivatalosan forgalombahozatali engedélyt az EMA-tól.
A folyamat felgyorsítása érdekében a gyógyszerügynökség megkezdte a Novavax amerikai és a német CureVac gyógyszeripari vállalatok által fejlesztett oltóanyagok, valamint csütörtökön az amerikai Eli Lilly gyógyszergyártó koronavírus elleni bamlanivimab és az etesemivab nevű gyógyszereinek folyamatos értékelését is.
A Johnson & Johnson vakcinájának európai uniós forgalmazását az EMA ajánlását követően az Európai Bizottságnak kell hivatalosan engedélyeznie.











