Kulcsfontosságú lépés az AIDS ellen
A humán immundeficiencia-vírus (HIV) életciklusa azzal veszi kezdetét, hogy a vírusrészecske külső burka egy végzetes "ölelésben" összeforr a gazdasejt sejthártyájával. E döntő pillanat megpecsételi az áldozatul esett immunsejt sorsát: a sikeres fúziót követően a vírus beléjuttatja örökítőanyagát, amely a sejtmagba kerülve akár évekig szunnyadhat, hogy aztán hosszú álmából felébredve újabb vírusrészecskéket termeljen, és elpusztítsa gazdáját.
Nem csoda, hogy a HIV-ellenes gyógyszerek elsődleges céljai közé tartozik a vírus és gazdasejtje közötti összeolvadás a gátlása. (A napjainkban alkalmazott HIV-ellenes terápia stratégiáiról keretes írásunkban olvashat.) Az AIDS felbukkanása óta intenzív kutatás tárgyai azok a fehérjemolekulák, amelyek egyfelől a vírusrészecske, másfelől a gazdasejt részéről aktívan részt vesznek a fúziós folyamatban. Ahhoz, hogy az összeolvadást gyógyszeresen gátolni lehessen, atomi léptékű felbontásban meg kell ismerni a benne szereplő fehérjék szerkezetét, mert csak így lehet olyan molekulákat tervezni, amelyek valamelyik partnerhez kötődve blokkolják a vírus-gazdasejt kapcsolatot. Míg a vírus kritikus burokfehérjéjének nagyfelbontású szerkezete már jó ideje rendelkezésre áll, a HIV áldozatául eső immunsejtek érintett felszíni fehérjéi, a normálisan a sejt-sejt kommunikációban szereplő CXCR4 és a CCR5 jelű kemokin-receptorok mindeddig nem adták meg magukat az elemzésnek. Ez részben e fehérjék sajátos, igen hajlékony szerkezetével magyarázható, amely megnehezíti, hogy az atomi felbontást biztosító röntgenkrisztallográfiás eljárás számára belőlük apró kristályokat állítsanak elő.
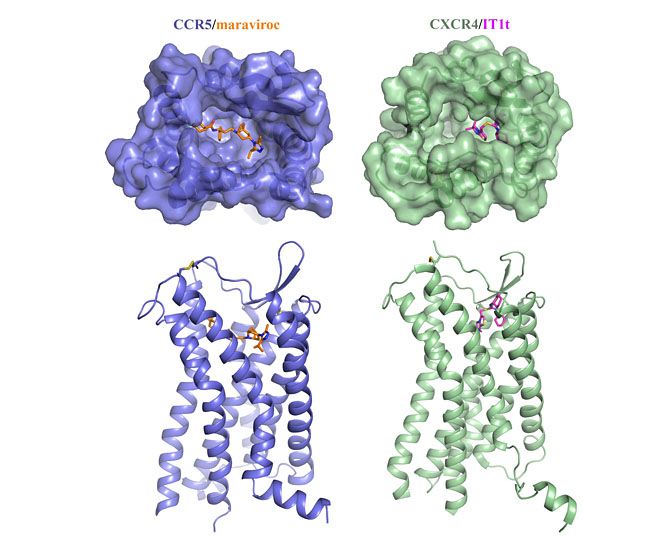
Ezen az áldatlan helyzeten változtatott egy kínai és amerikai tudósokból álló kutatócsoport, akik megtalálták a kulcsot előbb a CXCR4, majd legújabban a CCR5 vizsgálatához, és meghatározták mindkét fehérje atomi felbontású szerkezetét. A Science-ben frissen közölt cikkükben leírják, hogy CCR5-öt már a terápiás gyakorlatban lévő gátlószerével, a maraviroc-kal együtt kristályosították ki, így munkájukkal nemcsak magának a receptornak a szerkezetére, de a maraviroc pontos kötőhelyére és hatásmechanizmusára is fényt derítettek.
A tudományos közösség régóta várt erre az eredményre. A természetes HIV-variánsok tanulmányozásából, valamint maraviroc-kal és hasonló szerekkel kezelt betegek megfigyeléséből ismeretes volt, hogy a vírus váltogatva képes a CXCR4-et és a CCR5-öt használni a gazdasejtbe lépéshez, és ha egy csak az egyik vagy másik receptort gátló szerrel akadályozzák, hajlamos átváltani a másik belépési út használatára – és így kicsúszni a gyógyszer hatása alól. A CXCR4 és a CCR5 nagyfelbontású szerkezeteinek együttes ismeretében viszont már olyan gyógyszermolekulák tervezésére is lehetőség nyílik, amelyek bezárják ezt a kiskaput, és mindkét utat egyszerre vágják el a HIV elől.
A mostani áttörést korábbi kutatási eredmények hosszú sora előzte meg. Időbe tellett az is, míg egyáltalán kiderült, hogy a HIV elsőként azonosított partnere, a szintén többféle immunsejten feltűnő CD4 receptor mellett az összeolvadáshoz más gazdasejt-eredetű sejtfelszíni fehérjék is szükségesek. A CCR5 ilyen funkciója csak 1996-ban, tehát jó egy évtizeddel az intenzív HIV-kutatás megindulása után vált bizonyítottá.
Hogy a CCR5 receptor mennyire fontos szerepet tölt be a HIV-fertőzésben, azt alátámasztja a megfigyelés, miszerint egyes emberek, akik örökletesen a CCR5 egyes módosulatait hordozzák, fokozott, vagy éppen csökkent fogékonyságot mutatnak a HIV-re nézve, és ha megfertőződnek, a betegség lefolyása is eltér bennük a megszokottól. A CCR5 egy csonka változata, amely az európai népesség kb. 10 százalékában található meg, egyáltalán nem jelenik meg az immunsejtek felszínén – és azok, akik kizárólag ezzel a variánssal rendelkeznek, szinte teljes védettséget élveznek a HIV-fertőzéssel szemben. Amióta ez ismeretes, a tudósok folyamatosan próbálkoznak olyan HIV-ellenes szerek kifejlesztésével, amelyek megakadályozzák a vírus és a CCR5 közötti kapcsolat létrejöttét, vagy más módon teszik működésképtelenné a receptort. Ennek ellenére mindmáig alig néhány CCR5-gátlószert sikerült előállítani, és azok működési mechanizmusát sem ismerte pontosan senki. Mind az új szerek tervezéséhez, mind a létezők megértéséhez hiányzott eddig az a nagyfelbontású molekuláris „képmás”, amelyet a Science-cikk szerzői most előállítottak.
A kutatás motorja Beili Wu, a Kínai Tudományos Akadémia sanghaji Orvosi Anyagtudományi Intézetének professzora volt, aki az elmúlt hat évben fáradhatatlanul dolgozott a probléma megoldásán. A kutatónő 2007-ben érkezett a kaliforniai Scripps Research Institute-ba, Raymond C. Stevens laboratóriumába, hogy a CCR5 és a CXCR4 receptorok szerkezetét és működését tanulmányozza. Kezdetben a CXCR4 állt érdeklődése középpontjában, mert bár ezt a receptort a HIV-nek a ritkább változatai használják a gazdasejtbe való bejutáshoz – a leggyakoribb változat a CCR5-öt részesíti előnyben –, a CXCR4 szerkezetmeghatározása kevesebb technikai akadályt gördített az útjukba. Aztán, mikor 2010-ben a Science-ben megjelentették a CXCR4-gyel kapcsolatos eredményeiket, Wu visszatért a CCR5 lezáratlan ügyéhez. Mivel a CCR5-öt a maga ide-oda-csukló alakjával különösen problémás volt kristályszerkezetbe parancsolni, ötletes megoldással egy másik fehérjét fűztek hozzá, amely segített a kívánt szabályos elrendezés kialakításában.

A kristályosításhoz – az ilyen jellegű munkák esetében bevett módon – a vizsgálni kívánt fehérje gátlószerét is segítségül hívták, a gátlószerek ugyanis rendszerint merevebb formába kényszerítik célmolekulájukat. A CCR5 esetében a már 2007 óta forgalomban lévő maraviroc nevű HIV-ellenes gyógyszerre esett a választás. A röntgenkrisztallográfiás „pillanatfelvételt” ezért a CCR5-nek arról a formájáról készítették, amely – a maraviroc-kal komplexben – ellenáll a HIV-fertőzésnek. Járulékos eredményként megismerték a maraviroc pontos kötőhelyét is a CCR5-molekula felszínén, így nem mellesleg az is kiderült: a szer nem közvetlenül a vírus-burkofehérje kötőhelyét blokkolja, hanem a CCR5 egy másik régiójához kötődve úgy módosítja a teljes receptor alakját, hogy az alkalmatlanná válik a vírus fogadására.
Most már, hogy mind a CXCR4, mind a CCR5 finomszerkezete rendelkezésre áll, a kettő összehasonlításával lehetségessé vált annak megértése, miként képes a vírus a kór természetes lefolyása során, vagy a kezelés hatására egyikről a másikra „átkapcsolni”. Kezdetben a legtöbb HIV-fertőzöttben a vírus a CCR5-öt használja a bejutáshoz, idővel azonban legtöbbször átszokik a CXCR4-re. Ezzel a váltással egy sor addig nem fenyegetett sejttípus is a fertőzés célpontjává válik. Feltehetőleg ez az a pillanat, amikor a vírus terjedése annyira felgyorsul a szervezetben, hogy megjelennek a tényleges immunhiány – vagyis az AIDS – tünetei, s végül ez vezet el a beteg halálához. A CXCR4 és a CCR5 szerkezetének összevetéséből kiderül, hogy a vírus kötődési preferenciájának átkapcsolásához egészen finom változások is elegendőek, s ezen változások megismerése nagyban előre fogja lendíteni a gyógyszerek következő generációjának kifejlesztését. E jövőbeni szerek már egyszerre fogják akadályozni a vírusnak mindkét receptorhoz való kapcsolódását, s így remélhetőleg meggátolják a HIV-fertőzés végső stádiumának kialakulását.
A HIV-fertőzés gyógyításában jelenleg öt gyógyszerosztály tagjait alkalmazzák, amelyek a HIV életciklusának különböző fázisait gátolják. A fertőzési ciklus kezdetét, a vírusnak a gazdasejtbe való belépését akadályozzák a fúziógátló szerek. Ilyen a jelen cikkben is említett maraviroc, de ezt az osztályt jelenleg még kevés vegyület képviseli. A HIV-ellenes szerek két további osztálya, a nukleozid- és nem-nukleozid-típusú reverz transzkriptáz-gátlók a vírusnak azt a sajátságos enzimjét gátolják, amely a vírus RNS-ben tárolt genetikai anyagát a sejtmag DNS-nyelvére írja át. Az integráz-gátlók az életciklus következő lépésébe avatkoznak bele: abba, amikor a DNS-sé átírt örökítőanyagot a vírus a gazdasejt saját DNS-ébe beépíti. Végül a proteázgátlók a vírusnak azzal az enzimjével bánnak el, amely az szaporodni kívánó kórokozó új vírusrészecskéinek kialakulását, összeszerelődését gátolja. A vírus enzimei különösen kedvező támadáspontokat kínálnak a terápia számára, hiszen ehhez hasonló enzimaktivitások az ép emberi sejtek működéséhez nem szükségesek, tehát a kezelés viszonylag mellékhatásmentesen kivitelezhető. Ezzel együtt ma már sosem alkalmazzák egyik vagy másik gyógyszerosztály tagjait egyedül: a modern rutinban az egy vagy több osztályhoz tartozó szerek jól beállított kombinációit (kombinációs antiretrovirális terápia vagy CART) adják a HIV-fertőzötteknek, akik így lényegesen hosszabb tünetmentes életet élvezhetnek.











