Mengyelejev rendszere sem időtlen alkotás


Az utolsó, nemrég bekerült 118-as rendszámú oganesszonnal nem feltétlenül vált befejezetté a periódusos rendszer. Már jelenleg is folynak a kutatások az újabb, ennél is nehezebb elemek felfedezésére. Ha sikerül még további hármat felfedezni, azzal jelentősen átrajzolódik a periódusos rendszer kinézete.
A rendszer első ránézésre bonyolult tudományos eszköznek tűnhet, amit csak a tudósok értenek. A valóságban azonban egy egyszerű táblázat (amit angol neve jobban is sugall: Periodic Table, vagyis periódusos táblázat) benne az eddig felfedezett elemek vegyjelével, és néhány tulajdonságával.
A periódusos rendszer
Más kérdés persze, hogy ez a valaha készült egyik legfontosabb táblázat, amelynek nem is olyan nehéz dolog az áttekintése.
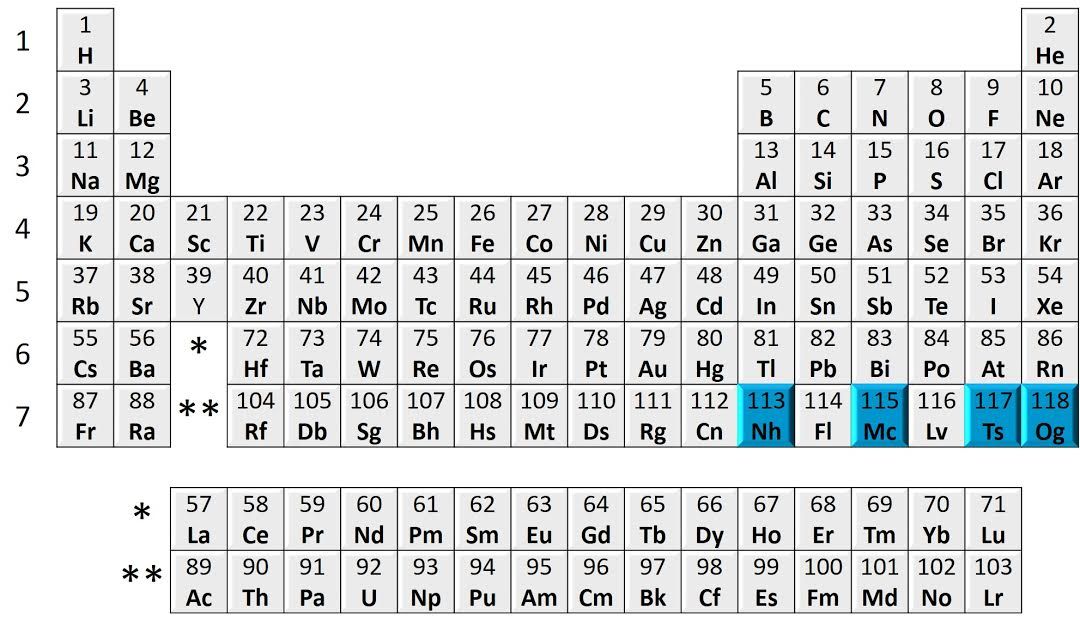
Alul két, látszólag magányos sort látunk. Ezek (lantanoidák és aktinoidák) azonban ugyan úgy részei a „felső" táblázatnak, pusztán praktikus okokból kerültek lentre. Csillaggal, vagy más szimbólummal jelölhetjük a fenti részen eredeti helyüket, ezáltal helyet spórolunk meg, és nem is lesz annyira széles az ábra.
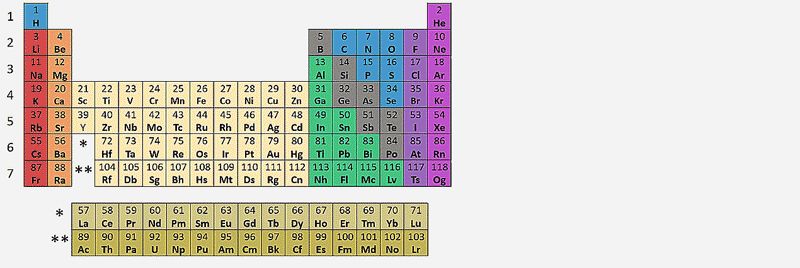
Az atomok elektronfelhője elektronhéjakból, az elektronhéjak pedig alhéjakból állnak.
A periódusos rendszer úgy épül fel, hogy tükröződik benne az alhéjak energetikai sorendje.
Így a táblázat az éppen beépülő alhéj alapján s-, p-, d-, és f-mezőkre tagolható. Ha követjük az úgynevezett „átlós szabályt", akkor néhány kivételtől eltekintve az elem rendszáma alapján megadható annak alapállapotú elektronszerkezete, ennek következtében pedig a periódusos rendszerben elfoglalt helye, mint például ezen a videón az első 20 elem esetében.
Minden új elektronhéj esetén egy új fajta alhéj is megjelenik. Ha ez igaz, akkor azonban nem csak a jól ismert s-, p-, d-, és f-alhéjak léteznek, hanem az 5. héjtól kezdődően már egy g-, a 6.-tól pedig egy h-alhéj is, és így tovább. Utóbbiakról azért hallunk ritkábban, mert még nem fedeztek fel olyan elemet, amelynek alapállapotú atomjának elektronjai közül bármelyiknek is szüksége lenne rájuk. Ennek megfelelően a periódusos rendszerben jelenleg nincs is g-, vagy éppen h-mező.

Az első elem, amelynek egyik elektronja már (elméletileg) egy g-alhéjra kerülne, az a 121-es rendszámú, vagyis az unbiunium.
Onnantól kezdve, hogy ezt sikeresen előállítják, új rész megnyitására lesz szükség a periódusos rendszerben, méghozzá a g-mező részére.
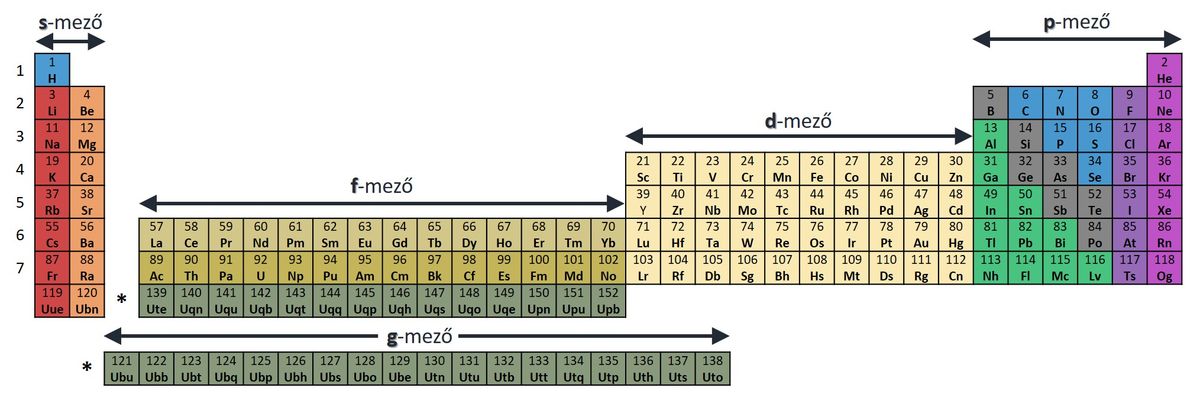
2050-re már ennél nagyobb rendszámú elemek is felfedezésre kerülhetnek, így a periódusos rendszer az úgynevezett szuperaktinoidákkal kiegészülve ekkora már máshogy fog kinézni.
Helytakarékossági szempontból persze ismét csak lehet az f-mezőt is alulra helyezni, a g-mezőhöz hasonlóan, eredeti helyét valamilyen más szimbólummal jelezve.
Már az első 20 elem esetén is van két kivétel az „átlós szabály" alól (a króm és a réz), tovább haladva a periódusos rendszerben pedig egyre több ilyen példát találni.
A g-mező elemeihez érve még jelentősebb eltérések várhatóak.
A tényleges (alapállapotú) elektronszerkezetek, ennek következtében a táblázat pontos kinézete némileg eltérhet majd a fenti képen láthatótól. A 139-es és 140-es rendszámú elemek helye különösen bizonytalan.
A periódusos rendszer még itt sem feltétlenül ér véget. Az egyik legoptimistább becslés szerint 173 elem létezését leszünk képesek igazolni, de akadnak olyanok is, akik nem látják akadályát végtelen számú elem létrehozásának sem.
• Megfelelő módszer hiánya
A szupernehéz elemek a természetben nem találhatóak meg, csak mesterségesen sikerült eddig előállítani ezeket, könnyebb atomok „összeolvasztásával". Ha léteztek is valaha, nagyon gyors felezési idejük miatt már rég elbomlott a teljes mennyiségük.
Éppen ezért a felfedezésük helyett sokkal inkább a feltalálásukról beszélhetünk.
A jelenleg használt módszerekkel már a mostani 4 új elemet is nagyon komplikált volt feltalálni. Az ezeknél nehezebb elemek előállítása még problémásabbnak ígérkezik. (Egyébként nem csak az elem tömege befolyásolja, hogy mennyire könnyű, vagy nehéz azt felfedezni, hanem az is, hogy páros vagy páratlan rendszámú-e.
A páros rendszámúakat általában könnyebb feltalálni, ezért van például az, hogy a 116-os rendszámú livermorium már régebb óta a periódusos rendszerben van, míg a könnyebb, de páratlan rendszámú 113-mas nihónium, és a 115-ös moszkóvium még csak most kerültek be végleges nevükkel). A kutatók úgy vélik, hogy a mostani eljárások legjobb esetben is csak a 119-es, és 120-as rendszámú elemek felfedezéséhez lesznek alkalmasak. Vagyis éppen a 121-es elemhez – ami az „új" periódusos rendszert tenné szükségessé – már szinte biztosan más módszereket kell fejleszteni.
• Gyors felezési idő
Az uránon túli elemek a rendszám (ezáltal a tömeg) növekedésével egyre rövidebb és rövidebb ideig életképesek.
Hacsak nem létezik a fizikusok által hőn áhított stabilitás szigete
– amely az elmélet szerint bizonyos mágikus nukleonszámok esetén a szupernehéz elemek között lehet egy olyan „sziget", ahol egész hosszú felezési idejű elemek is lehetnek – ez a trend nem fog változni.
Nem elég azonban az, ha csak létrejönnek, de annyi ideig életképesnek is kell maradniuk, amíg észlelni tudjuk őket. Ez legrosszabb esetben is minimum 10-14-en másodperces időintervallumot jelent. Legalább ennyi ideig kell ugyanis stabilnak lennie egy elemnek ahhoz, hogy létezővé nyilvánítsák. Ez emberi ésszel felfoghatatlanul rövid idő, ezeknek az szupernehéz elemeknek azonban mégis elég hosszú ahhoz, hogy alig éljék meg ezt a „kort".
Az újabb és újabb elemek feltalálására tett törekvések igen drágák, és a sikerek ellenére mégis haszontalannak tűnhetnek. Nem valószínű, hogy az életben is használható, minden eddiginél erősebb szerkezeti anyagot, vagy az ezüstnél is jobb elektromos vezetőt sikerül feltalálni. A szupernehéz elemek létrehozása azonban mégsem csak a kutatók költséges játéka.

Ha sikerül (nagyon gyorsan) megfigyeléseket, méréseket végezni az előállított atomokon, az a jelenlegi tudásunkat bővítheti az anyagot felépítő apró részecskékkel kapcsolatban. Így közvetve ugyan, de hozzájárulhatnak az új elemek életminőségünk javításához.
(A cikk szerzője, Varga Szabolcs, a BioKemOnline – biológia és kémia érettségi portál - szerkesztője.)











