Megfejtették, hogyan alakul ki a legrettegettebb agydaganat
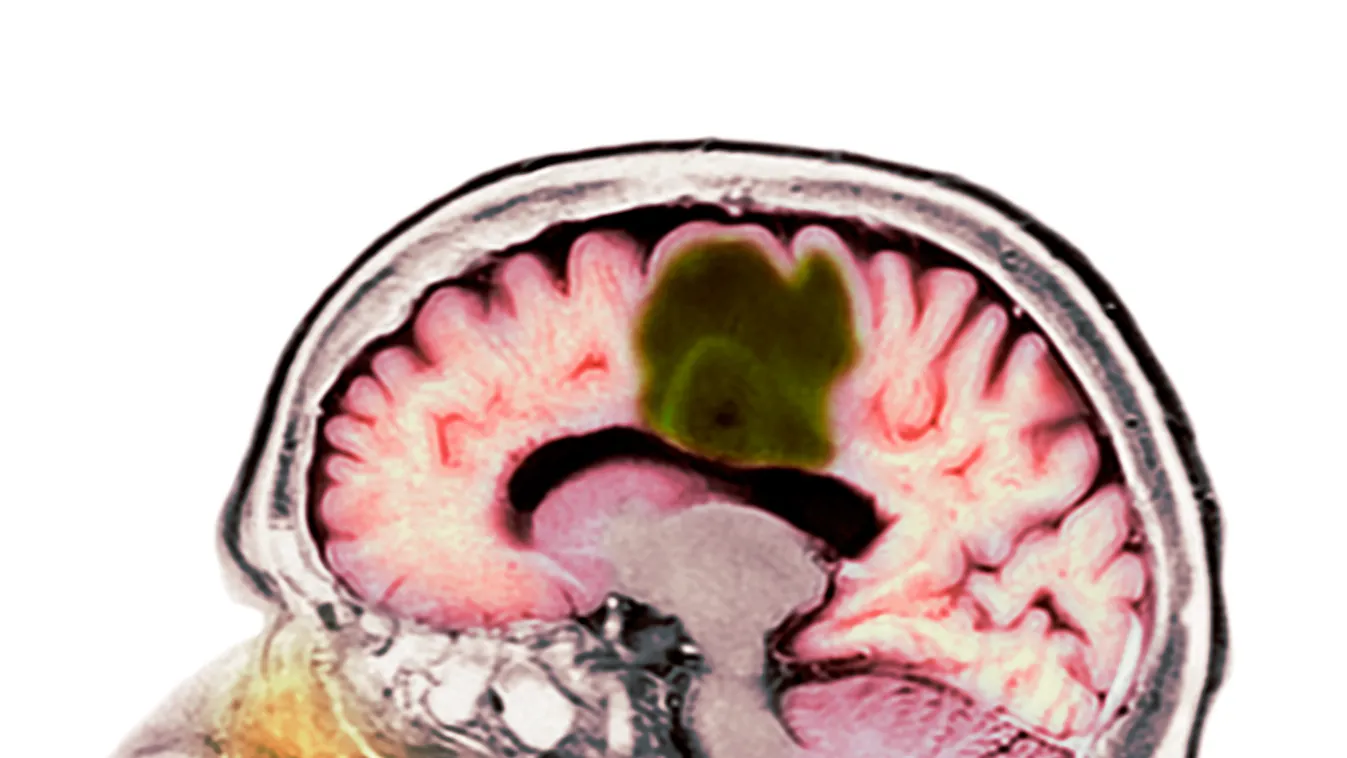

Az agyállomány sérülését követő gyógyulási folyamat daganatkeletkezésbe torkollhat, ha olyan mutáns sejtek vesznek részt az elvesztett szövet pótlásában, amelyek letérnek a normális sejtérés vágányáról – ismerték fel a Torontói Egyetem kutatói. A sérülést az ütéstől a fertőzésen át a stroke-ig a legkülönbözőbb behatások kiválthatják.
A felfedezés egy interdiszciplináris kutatócsoport munkáját dicséri, melynek tagjai a Torontói Egyetemen kívül a The Hospital for Sick Children (SickKids) gyermekkórházban, illetve a Princess Margaret Cancer Centre onkológiai központban dolgoznak, és a Stand Up To Cancer Canada Dream Team (kb.: Állj ki a rák ellen kanadai álomcsapat) kötelékében a glioblasztóma néven ismert, sajnálatosan gyakori agydaganattal foglalkoznak.
Adataink alapján azt valószínűsítjük, hogy ha az agy jól körülírható sejtjei egy bizonyos fajta mutációs mintázatot mutatnak, a sérülés olyan változásokat indíthat meg bennük, amely végül daganat keletkezéséhez vezet"
– mondta el Dr. Peter Dirks, a SickKids idegsebészeti osztályának, illetve fejlődés- és őssejtbiológiai programjának vezetője, továbbá a Dream Team irányítója. A Nature Cancer folyóiratban publikált kutatás vezetői között szerepelt még Gary Bader, a Torontói Egyetem orvosi karán működő Donnelly Sejt- és Biomolekuláris Kutatóközpont molekuláris genetika professzora, valamint Dr. Trevor Pugh, a Princess Margaret onkológiai központ szenior kutatója.
Az eredmények nyomán új terápiás opciók születhetnek a glioblasztóma kezelésére.
A leggyakoribb agydaganat-típus kezelési lehetőségei jelenleg rendkívül korlátozottak, és a betegek átlagos túlélése a diagnózis felállításától számítva mindössze 15 hónap.
A glioblasztómára gondolhatunk úgy, mint egy sebre, amely sosem gyógyul be
– magyarázza Dirks. – Izgalommal tölt el minket annak felderítése, mit mond el ez a megközelítés a daganat keletkezéséről és növekedéséről, és milyen új utakat nyit a kezelésben, ha a sérülésre és a gyulladásos válaszra összpontosítunk."
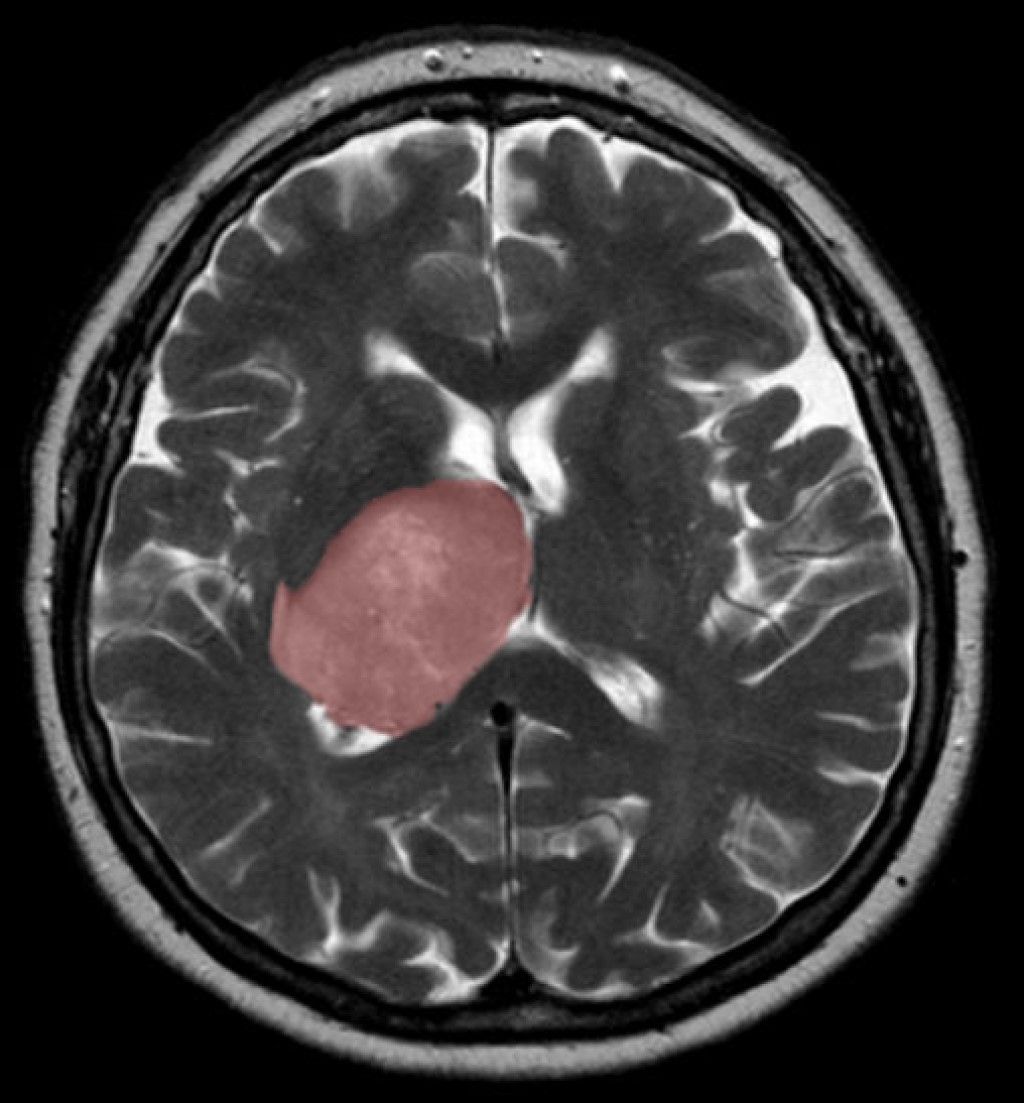
A kutatók a legmodernebb egysejt-RNS-szekvenálási és gépi tanulási technológiákat alkalmazták a glioblasztóma-őssejtek molekuláris feltérképezésére. Dirks csoportja korábban már bizonyította, hogy ezek az őssejtek felelősek a tumor keletkezéséért és a kezelés utáni kiújulásáért.
A vizsgálatok során a glioblasztóma-őssejtek olyan eddig ismeretlen alpopulációit azonosították, amelyek a daganatokon belül keverten helyezkednek el más daganat-őssejtekkel, de a gyulladás megkülönböztető molekuláris jegyeit viselik magukon.
Ebből arra következtettek, hogy a glioblasztómáknak legalábbis egy része akkor indul növekedésnek, amikor a sérült idegszövet önregenerációs folyamata, amely az elvesztett sejtek pótlására szolgál, mutációk miatt félresiklik. Ezek a korai események feltehetőleg évekkel az első tünetek megjelenése előtt történnek
– tette hozzá Dirks.
Amikor egy mutáns sejt bekapcsolódik a regeneráció folyamatába, az elszenvedett génhibái miatt nem tud leállni az osztódással, ugyanis a normális fékek és ellensúlyok rendszere felborult benne.
A célunk, hogy olyan gyógyszert találjunk, amely elpusztítja a glioblasztóma-őssejteket
– szögezte le Bader, akinek a doktorandusz-hallgatója, Owen Whitley végezte a számítógépes adatelemzést. – Ehhez azonban előbb ki kell ismernünk ezeknek a sejteknek a molekuláris természetét, mert csak így tudjuk őket hatékonyan megcélozni."

A kutatócsoport 26 beteg daganatából gyűjtött glioblasztóma-őssejteket, és a laboratóriumban felszaporították őket annyira, hogy az elemzésekhez szükséges mennyiség rendelkezésre álljon ezekből a ritka sejtekből. Közel 70 ezer sejtet vetettek alá egysejt-RNS-szekvenálásnak, amely technika alkalmas arra, hogy minden egyes sejt egyedi génkifejeződési mintázatát – a gének be- vagy kikapcsolt állapotát – feltérképezze. Ezt az aprólékos és időigényes munkát Pugh laboratóriumának egyik doktorandusza, Laura Richards irányította.
Az adatok megerősítették azt a korábbi feltételezést, hogy ezek a daganatok extrém mértékű belső heterogenitást mutatnak, vagyis valamennyi daganat jelentős számú, molekuláris szinten jól elkülönülő őssejt leszármazottainak keveréke.
A daganat visszatérése a kezelés után azért olyan gyakori, mert a jelenlegi kezelések nem képesek e rendkívül sokféle sejtpopuláció mindegyikét kiirtani.
A génkifejeződési mintázatok azt mutatták, hogy a glioblasztómák két jól elválasztható molekuláris állapot, a „fejlődési" és a „sérülésre adott válasz" valamelyike felé tendálnak. Minden beteg daganata elhelyezhető valahol e két végpont közti skálán. A „fejlődési" állapot a glioblasztóma-őssejtek jellegzetes ujjlenyomata, amely hasonlít az embrionális agyat az egyedfejlődés során felépítő, gyorsan osztódó idegi őssejtekére. Ennek a mintázatnak a jelenléte tehát nem lepett meg senkit. A „sérülésre adott válasz" mintázatra azonban nem számítottak a kutatók. Erre az állapotra az immunológiai jelútvonalak és gyulladásos molekulák, például az interferon és a TNF-alfa felszabályozódása jellemző, ami a sebgyógyulás folyamatára emlékeztet. Ennek a sajátos immunológiai mintázatnak a felderítése egyértelműen az egysejt-technológia érdeme, ugyanis a régebbi, sok sejtet kiátlagoló génkifejeződési vizsgálatok nem bukkantak a nyomára.
Mindeközben a Leslie Dan Gyógyszerészeti Karon Stephanie Anger laboratóriumában zajló kutatások kiderítették, hogy a kétféle állapot – a fejlődési és a gyulladásos – más és más gének kiütésére reagál érzékenyen.
Ezzel egy sor olyan potenciális gyógyszercélpontot azonosítottak, amelyek a gyulladással kapcsolatosak, és korábban senki sem gondolt rájuk a glioblasztómával összefüggésben.
A kétféle állapot relatív hozzájárulása a daganat génkifejeződési profiljához betegspecifikusnak bizonyult, és minden egyes tumor a két végpont közötti skála egyik vagy másik végpontja felé mutat eltolódást. A kutatók most azt vizsgálják, miként használhatnák ki a daganatok ilyen vagy olyan irányú elköteleződését a célzott terápia során. „Olyan gyógyszereket keresünk, amelyek a skála különféle pontjain álló daganatok ellen hatékonyak – fejtette ki Pugh, aki egyben az Ontario Institute for Cancer Research genomikai részlegének igazgatója. – Valódi esély kínálkozik itt a precíziós medicína számára: a betegek daganatait az egyes sejtek szintjére lebontva elemezhetjük, és olyan gyógyszerkombinációkat tervezhetünk, amelyek egyidejűleg több daganatőssejt-populációt is kiiktatnak."